2020 год оказался крайне непростым, как для системы здравоохранения, медицинской промышленности, так и для экономики в целом. Не смотря на беспрецедентно высокий спрос на средства индивидуальной защиты, медизделия для лабораторной диагностики и реанимационное оборудование, реальное мировое производство всей медицинской техники в 2020 году снизилось на 1,8%, по сравнению с 2019 годом. Падение производства медицинского оборудования, как и других отраслей экономики, объясняется локдауном, переориентацией части производств и закрытием границ, в результате которого появились сложности с поставками комплектующих.
По мнению экспертов, по итогам 2020 года объем мирового рынка медицинских изделий (МИ) составит около 411,4 млрд. USD, что на 3,2% ниже показателя 2019 года. Топ-10 международных компаний производителей медицинских изделий по версии Proclinical представлено на рисунке ниже.
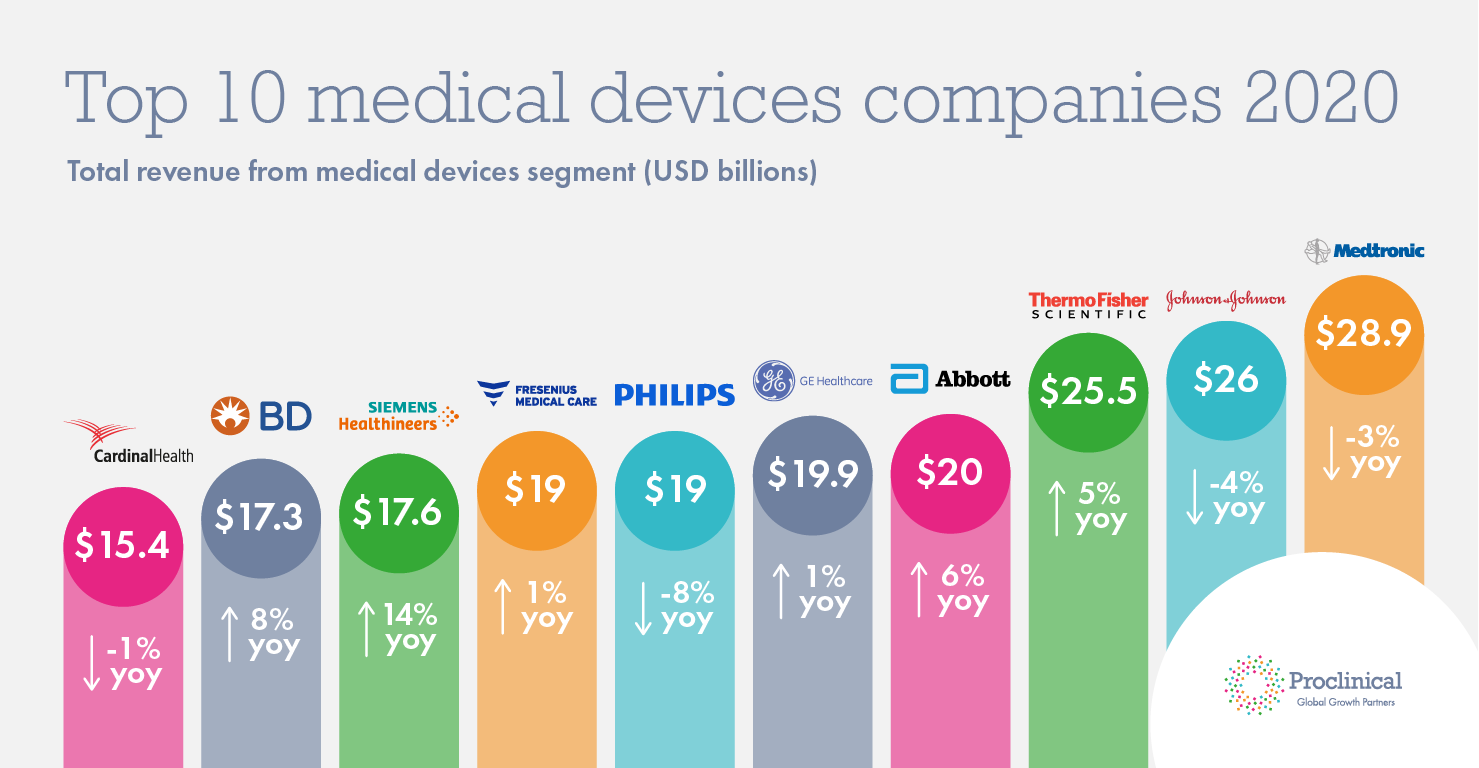
Доля российского рынка медизделий занимает около 1,3% от мирового. Объем производства медицинской техники в России в 2020 году сократился на 5,2% по сравнению с 2019 годом.
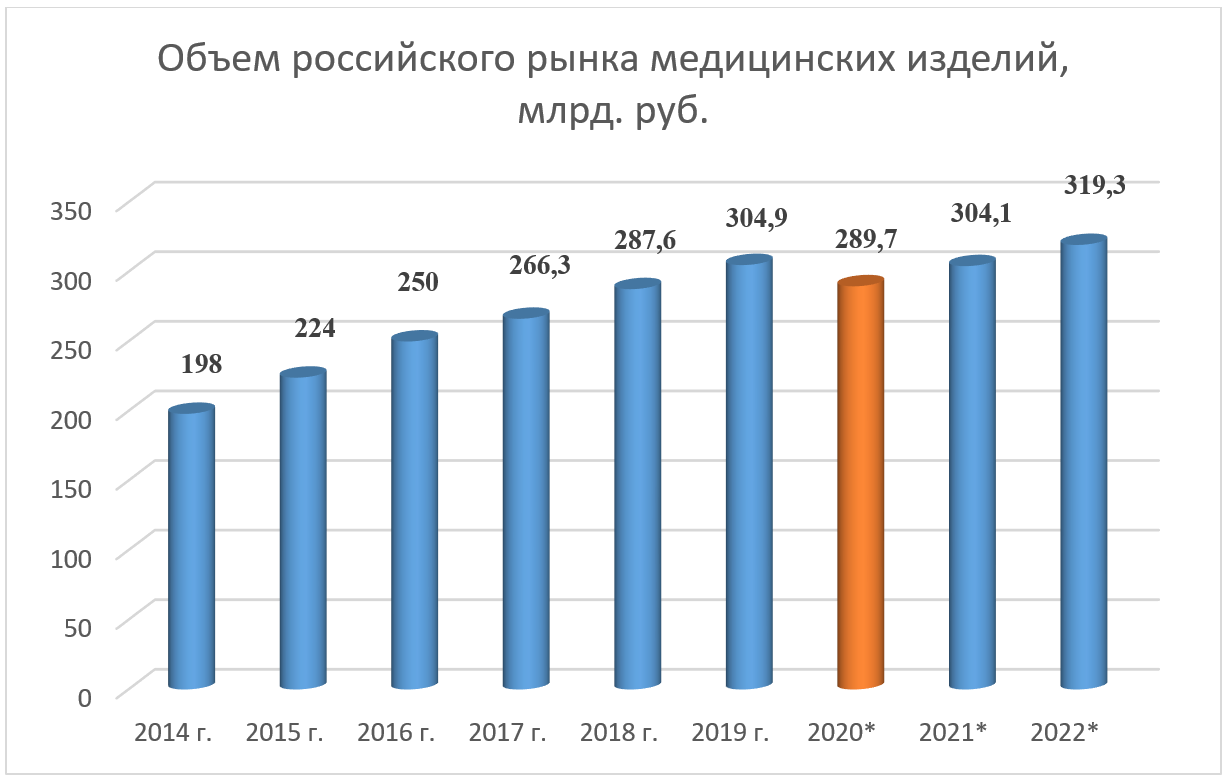
Не смотря на падение объемов в большинстве сегментов рынка медицинского оборудования, существенно выросла доля сегментов медизделий для реанимации, лабораторной (in-vitro) диагностики и общебольничного оборудования.
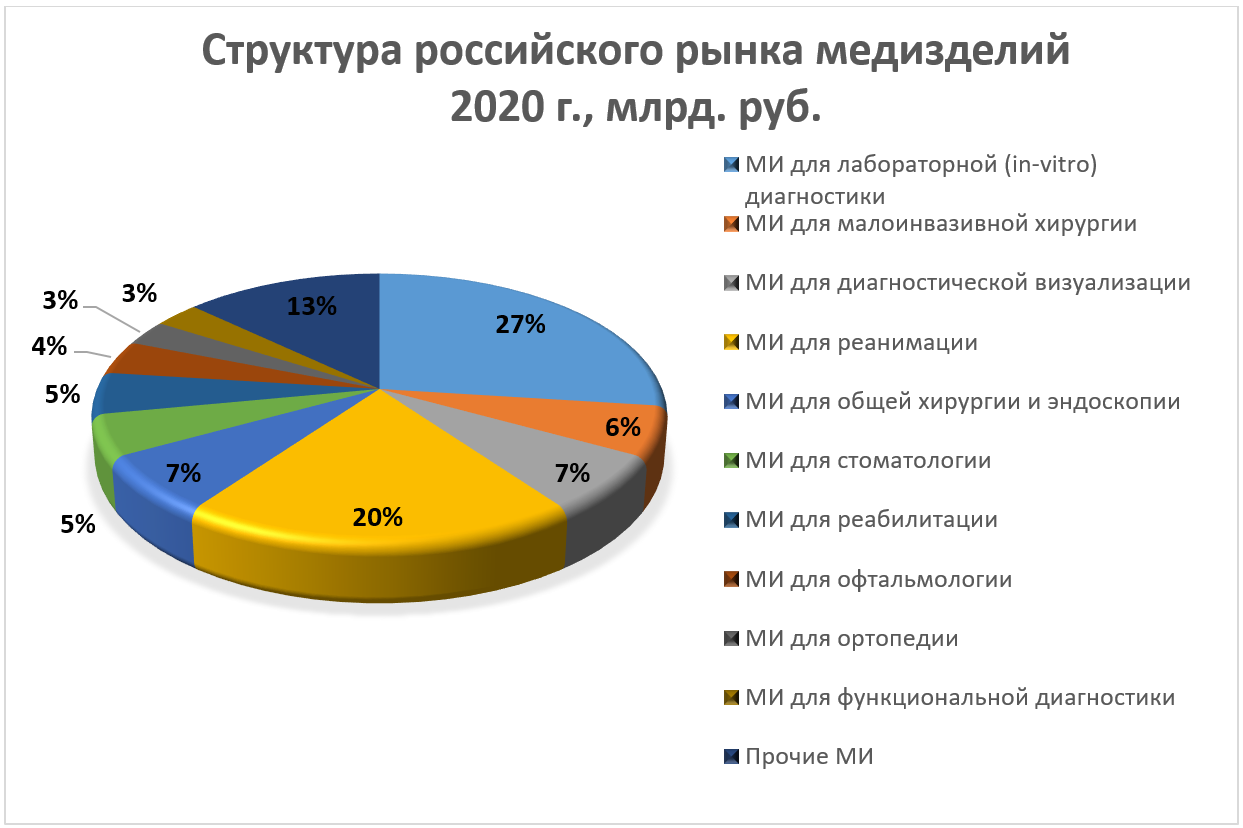
За первые семь месяцев 2020 года экспорт российских медицинских изделий составил $ 673,32 млн. Наибольшая доля экспорта приходилась на маски, дыхательное оборудование, термометры, рентгенодиагностическое оборудование, дефибрилляторы и аппаратуру для переливания крови. Доля импорта медизделий, по сравнению с 2019 годом, снизилась на 6,5%.
Опыт пандемии коронавируса наглядно продемонстрировал необходимость увеличения затрат не только на здравоохранение, но и на разработки в области медицины для наращивания производства конкурентоспособного медицинского оборудования. По прогнозам экспертов, в 2021 году, медицинская промышленность в России может не только восстановиться, но и вырасти по отношению к 2020 году на 5-6%.
Помимо существенных изменений в объеме и структуре российского рынка медицинских изделий, в 2020 году было принято большое число нормативно-правовых актов с высокой степенью регулирующего воздействия:
1. Введение упрощенной процедуры регистрации для медизделий, предназначенных для борьбы с эпидемией коронавируса
18 марта 2020 года Постановлением Правительства №299 был введен ускоренный порядок регистрации для изделий с низкой степенью потенциального риска применения (респираторов, медицинских масок, изолирующих халатов и костюмов, а также перчаток и бахил). Для первичной регистрации заявителю необходимо было предоставить в Росздравнадзор копию документа, подтверждающего его полномочия, техническую и эксплуатационную документацию, фотографии общего вида медизделия и опись документов. В случае отсутствия претензий, ведомство в течение пяти дней должно было выдать регистрационное удостоверение. Затем, в течение 150 дней заявитель должен был представить полный пакет документов на данное медицинское изделие, включая заключение о клинических, токсикологических и технических исследованиях, выполненных на базе ФГБУ «ВНИИИМТ» Росздравнадзора, и подтверждение качества и безопасности вещества, из которого произведено изделие.
3 апреля 2020 г. было подписано Постановление Правительство № 430, согласно которому временные регистрационные удостоверения на тест-системы, аппараты искусственной вентиляции легких (ИВЛ) и ряд другой медицинской техники должны были выдаваться за три дня. А одноразовые медизделия (медицинские маски, халаты, перчатки и бахилы) были освобождены от регистрации Росздравнадзором на время эпидемии в случае, если они зарегистрированы в стране-изготовителе.
В июне Постановлением №804 «О внесении изменений в особенности обращения медицинских изделий, в том числе государственной регистрации серии (партии) медицинского изделия», перечень медицинских изделий, подпадающих под упрощенную регистрацию, был расширен до 363 видов. В него вошло оборудование и расходные материалы для лабораторной диагностики, медицинская мебель, холодильные установки, дыхательные контуры, коннекторы и клапаны для ИВЛ, мониторы пациентов, пульсоксиметры, бронхоскопы, аспирационные системы, бактерицидные лампы и другие медизделия.
По сообщению Росздравнадзора, на начало декабря 2020 года по Постановлению Правительства №299 было зарегистрировано 1 342 медицинских изделий. Помимо этого, разрешение на обращение получили 203 набора для диагностики COVID-19 и антител к коронавирусу, 11 разрешений на обращение было выдано на аппараты искусственной вентиляции легких, еще 7 на термометры и 1 на функциональные кровати.
Первоначально срок получения регистрационных удостоверений по упрощенной процедуре был ограничен 2020 годом, однако, 13 ноября Михаилом Мишустиным было подписано постановление о продлении действия постановления до 1 января 2022 года.
В тоже время, по словам заместителя руководителя Росздравнадзора Дмитрия Павлюкова, из общего количества медизделий, зарегистрированных по Постановлению №299, процедуру подтверждения соответствия прошли только 12 поставщиков. В результате, около 20 регистрационных удостоверений уже отменены, в связи с истечением срока доказательства качества, безопасности и эффективности медицинского изделия.
Росздравнадзор совместно с Минздравом России рассматривает вариант внесения корректировок в данное Постановление.
2. Регистрация медицинского программного обеспечения, в том числе с использованием искусственного интеллекта
Первые изменения нормативно-правового поля в данном вопросе произошли в феврале, когда Росздравнадзором было опубликовано информационное письмо № 02И-297/20 «О программном обеспечении», содержащее критерии отнесения программного обеспечения (ПО) к медицинским изделиям.
Кроме того, в апреле 2020 года была зарегистрирована первая система поддержки принятия врачебных решений с искусственным интеллектом (ИИ) — Webiomed, компании «К-Лаб».
Затем, в июне Президент России Владимир Путин поручил провести широкую цифровизацию и активнее внедрять технологии искусственного интеллекта в медицине.
А в августе эксперты Центра диагностики и телемедицины Департамента здравоохранения Москвы совместно с подкомитетом «Искусственный интеллект в здравоохранении» представили проект первого национального стандарта ГОСТ Р, который будет регулировать проведение клинических испытаний медицинских систем искусственного интеллекта (СИИ) в России. Еще 6 стандартов, посвященных СИИ в клинической медицине, находятся в разработке.
Дорожная карта, предусматривающая план перевода бюджетного здравоохранения на работу с искусственным интеллектом была утверждена в ноябре 2020 года. Предполагается, что в каждой бюджетной организации должно появиться не менее пяти видов изделий и сервисов со встроенным искусственным интеллектом.
Кроме того, для повышения доступности умных технологий планировалось создать специальную отраслевую платформу, которая объединит в себе обезличенные медицинские данные пациентов из Федеральной интегрированной электронной медицинской карты Единой государственной информационной системы в сфере здравоохранения (ЕГИСЗ) для обучения программ на основе технологий искусственного интеллекта. И, как рассказал руководитель Центра компетенций цифровой трансформации сферы здравоохранения Минздрава РФ Михаил Левин на конференции «Медицина и качество – 2020», на начало декабря ЕГИСЗ уже сформировано 1,4 млрд обезличенных записей о пациентах для обучения искусственного интеллекта.
Также в ноябре было подписано Постановление Правительства №1906 об ускоренной (одноэтапной) регистрации программных продуктов, в том числе с применением технологий искусственного интеллекта, в качестве медицинских изделий. Речь идет о цифровых программах, которые используются для помощи врачам в диагностике онкологических заболеваний, планировании техники проведения хирургических операций, мониторинге состояния здоровья пожилых пациентов с хроническими заболеваниями, реабилитации больных.
А в конце декабря Приказом Минздрава РФ № 1236н были утверждены требования к содержанию технической документации на программное обеспечение, являющееся медизделием.
3. Изменения в области государственных закупок медицинских изделий
В 2020 году было принято несколько протекционистских законодательных актов, ограничивающих доступ к государственным закупкам иностранных производителей медизделий.
В соответствии с Федеральном законом от 31.07.2020 № 249-ФЗ «О внесении изменений в Федеральный закон «О контрактной системе в сфере закупок товаров, работ, услуг для обеспечения государственных и муниципальных нужд», вводится ежегодная минимальная доля закупок продукции из стран ЕАЭС.
Теперь Правительство РФ будет устанавливать перечень товаров, описание характеристик и порядок формирования начальной максимальной цены, а также перечень поставщиков товаров из ЕАЭС для выполнения минимальной доли закупок. А государственные заказчики до 1 апреля обязаны будут опубликовать в Единой информационной системе в сфере закупок отчет о выполнении минимальной доли, либо обоснование невозможности достижения квоты приобретения отечественных товаров.
Согласно, проекту Минпромторга России, утверждающему минимальную долю госзакупок продукции на 2021 — 2023 годы, доля медицинских изделий будет меняться из года в год. Например, для клейких перевязочных материалов, в том числе пропитанных или покрытых лекарственными средствами, и шприцов-инъекторов в 2021 году она составит 45% и будет увеличиваться на 10 п.п. в год. Для интраокулярных линз доля на 2021 год составит 35% (45% на 2022 год и 55% на 2023), для пробного набора очковых линз – 22% (32%, 42%).
Госзаказчики будут обязаны закупать не менее 18% емкостей для проб для исследований из стран ЕАЭС и 90% медицинской марли. Доля эндопротезов суставов из ЕАЭС должна будет составить в 2021 году не менее 10% (15% и 20% в 2022 и 2023 годах), имплантатов для остеосинтеза – 53% (58%, 63%), ортопедических стелек – 55% (57%, 60%).
Кроме того, в апреле 2020 года действие правила «Третий лишний» было расширено на медицинскую мебель, а также протезы, ортопедические изделия и их составные части. А в июле допуск к отечественному госзаказу ограничили еще и для производителей протезов синовиальной жидкости, применяемых в лечении ревматологических заболеваний.
В настоящее время Перечень, на который распространяется Постановление №102, включает более 140 видов медицинских изделий.
В декабре Правительство РФ установило квоты на госзакупки продукции российского происхождения по 223-ФЗ для двадцати профилей медицинских изделий. В перечень вошло рентгенологическое оборудование, компьютерные и магнитно-резонансные томографы, ультразвуковые сканеры, аппараты искусственной вентиляции легких и эндоскопическое оборудование.
Минимальная доля российской продукции в сегменте электрического диагностического и терапевтического оборудования для облучения, была установлена на уровне 9% в 2021 году, с ростом до 10% в 2022-2023 годах. При этом минимальная доля закупок российских КТ должна в 2021 году составить 50% с ростом до 75% в 2023 году, маммографов, рентгеновского оборудования и C-дуг – 55% в 2021 году с ростом до 75% в 2023 году.
Российские МРТ должны составлять не менее 30% от общего объема закупок в 2021 году с ростом до 50% в 2023 году. Квота для эндоскопического оборудования установлена в 55% в 2021 году с ростом до 75% в 2023 году. В случае ОФЭКТ и гамма-аппаратов минимальная доля на 2021 год составляет 40%, в 2023 году она должна составить 60%.
Для УЗИ доля закупок российской продукции установлена в 60% на 2021 год, дефибрилляторов, аппаратов ИВЛ и комплектующих к ним – 50%. Наибольшие минимальные доли на 2021 год установлены для медицинских морозильников – 65%, паровых стерилизаторов – 70% и медицинской марли – 90%.
В конце декабря Минпромторг России подготовил проект Постановления Правительства РФ «Об установлении запрета на допуск электронной продукции, происходящей из иностранных государств». Согласно которому, запрет на допуск к рынку госзаказа распространяется на всю продукцию под кодом ОКДП2 «26», за исключением медицинских изделий, в отношении которых ограничения были ранее установлены по правилу «Третий лишний». Среди оборудования, которое попадает под ограничения: КТ с разрешением 128 срезов и выше и МРТ. Для закупки такой продукции, произведенной за пределами ЕАЭС, заказчикам необходимо будет обращаться за разрешением в Минпромторг России.
Кроме того, был введен запрет на закупку иностранных медицинских масок на рынке госзаказа до конца 2021 года. Как ранее сообщал Минпромторг Россиии, за первое полугодие 2020 года 80% поставок медицинских масок пришлось на продукцию из стран Юго-Восточной Азии. При этом, объем производства масок в России с начала марта 2020 года вырос в 20 раз и составляет около 21 млн масок в сутки, при расчетной потребности госучреждений в 10,8 млн масок в сутки. В результате, сумма остатков на складах составляет около 141 млн медицинских масок, а некоторые предприятия вынуждены прекратить производство, в связи с отсутствием спроса.
Помимо введения дополнительных ограничений для медицинских изделий иностранного происхождения, в 2020 году были внесены изменения и в саму систему проведения государственных закупок. Так в августе был утвержден новый порядок формирования начальной максимальной цены контракта. Начальная максимальная цена контракта для медицинского оборудования, при эксплуатации которого нужны расходные материалы, теперь должна учитывать стоимость гарантийного обслуживания, комплектующих и расходников.
4. Другие значимые изменения в области обращения медицинских изделий
Резкое обострение эпидемиологической ситуации весной 2020 года послужило поводом для разработки Правительством РФ правил установления предельных отпускных цен и надбавок на медицинские изделия в условиях чрезвычайной ситуации, возникновения угрозы распространения опасного для окружающих заболевания или в случае резкого подорожания данной продукции.
В то же время Советом Евразийской экономической комиссии было принято решение об освобождении от ввозной таможенной пошлины товаров, используемых для предупреждения и предотвращения распространения коронавирусной инфекции. А в октябре 2020 года тарифная льгота была продлена до 31 марта 2021 года, за исключением ряда товаров, по которым уже налажено собственное производство в достаточном количестве.
Кроме того, в России был создан Консорциум разработчиков и производителей медицинской техники. Основополагающей целью его создания стала необходимость локализации основных видов медицинского оборудования на территории России, в связи возникающими рисками и угрозами. Производимые медицинские приборы будут вноситься в реестр российского радиоэлектронного оборудования в целях предоставления этой продукции дополнительных преференций после ее выхода на рынок. Опорным регионом для Консорциума разработчиков и производителей медицинской техники стала Свердловская область.
В июле было подписано Постановление Правительства № 982 о «регуляторной гильотине» в области контроля за оборотом медицинских изделий. Среди документов, действие которых будет аннулировано с 1 января 2021 года: постановление Правительства РФ №1360 от 12 декабря 2015 года «Об отдельных вопросах противодействия обороту фальсифицированных, недоброкачественных и контрафактных медицинских изделий», приказы Минздрава РФ №12н от 20 июня 2012 года «Об утверждении Порядка сообщения субъектами обращения медицинских изделий обо всех случаях выявления побочных действий» и №175н от 14 сентября 2012 года «Об утверждении Порядка осуществления мониторинга безопасности медицинских изделий».
Кроме того, было утверждено Постановление от 11 июля 2020 года №1027 о ежегодном пересмотре перечня медицинских изделий, освобожденных от НДС, согласно которому Минздрав России, Минпромторг России и Федеральная таможенная служба будут ежегодно, в срок до 15 февраля, проводить анализ применения перечня медицинских изделий, не подлежащих обложению налогом на добавленную стоимость, и при необходимости вносить в кабинет министров предложения о его корректировке.
Обновление сервисов Государственной информационной системы промышленности осенью 2020 года позволило подавать заявку и получать заключение о статусе промышленной продукции, как продукции, произведенной на территории Российской Федерации, полностью в электронном виде.
Пандемия коронавируса существенно обострила проблему утилизации медицинских отходов. С 2010 года вся сфера обращения с медицинскими отходами регулировалась СанПином «Санитарно‑эпидемиологические требования к обращению с медицинскими отходами». Медотходы в СанПине поделены на пять классов, и только отходы класса «Г» ставились в один ряд с отходами 1–4 класса опасности, требующими лицензирования и подпадающими под ФЗ-89 «Об отходах производства и потребления».
По оценкам операторов «мусорного» рынка, от 50% до 90% инфицированных или потенциально инфицированных медицинских отходов (класса «Б» и «В») не утилизируются должным образом, а захораниваются на несанкционированных площадках.
В 2020 году депутатами Госдумы был разработан проект поправок в существующее законодательство, которым вводится лицензирование деятельности в сфере обращения с медицинскими отходами «от накопления до транспортировки, обеззараживания и так далее».
В заключении хотелось бы отметить, что, не смотря на все изменения нормативно-правовой сферы, эпидемиологической и экономической ситуации в стране, которые принес 2020 год, Росздравнадзор еще в сентябре напомнил о необходимости замены регистрационных удостоверений на изделия медицинского назначения и медицинскую технику бессрочного действия до 1 января 2021 года.
Кроме того, проекту поправок в 323-ФЗ «Об основах охраны здоровья граждан», вводится требование об обязательном соответствии производства медицинских изделий системе менеджмента качества в зависимости от потенциального риска их применения.
С января 2021 года регистрация медицинских изделий, не подпадающих под упрощенную процедуру, должна будет осуществляться по требованиям ЕАЭС, включающим также включающим обязательное инспектирование производства. Первое регистрационное удостоверение на медицинское изделие в рамках ЕАЭС с первичным инспектированием производства, на предмет соответствия требованиям к внедрению, поддержанию и оценке системы менеджмента качества, было выдано в сентябре 2020 года.
5. Государственные программы и поддержка инноваций
В октябре 2020 года Минпромторг России предложил внести изменения в госпрограмму «Развитие фармацевтической и медицинской промышленности».
Согласно проекту документа, доля медицинских изделий отечественного производства в общем объеме потребления к 2024 году должна быть увеличена до 30% (в денежном выражении). Экспорт лекарственных средств и медицинских изделий должен достичь не менее 180 млрд рублей. А доля организаций, осуществляющих технологические инновации в медицинской и фармацевтической отрасли, в общем количестве производителей должна достичь 56%.
Кроме того, были сформированы правила предоставления в 2021 году бюджетным учреждениям грантов в форме субсидий из федерального бюджета на реализацию проектов по разработке медицинских изделий и лекарственных препаратов. Объем бюджетных ассигнований на данные цели составит 2,6 млрд рублей. Предельная сумма одного гранта — не более 260 млн рублей. Получатели грантов будут отбираться в результате конкурсов, проводимых Минпромторгом России. Для того чтобы претендовать на получение гранта, необходимо предоставить бизнес-план проекта, план-график его реализации и технико-экономическое обоснование (ТЭО) затрат.
В декабре 2020 года был утвержден перечень современных технологий, на основании которого будут заключаться специальные инвестиционные контракты (СПИК). В список попало более 600 перспективных технологий из различных отраслей, в том числе медицинской и фармацевтической промышленности, а также биоинженерии.
Компании смогут заключить с государством контракт, который предусматривает запуск серийного производства современной конкурентоспособной продукции. Государство со своей стороны гарантирует такому инвестору стабильные условия хозяйственной деятельности, а также налоговые льготы и преференции при проведении госзакупок, аренде земельных участков.
С января 2021 года начнется реализация проекта по переоснащению клиник по программе модернизации первичного звена здравоохранения, старт которой был отложен из-за эпидемии коронавируса. В итоговый список для переоснащения медучреждений вошло 121 наименование МИ. Согласно одобренным региональным программам, в период с 1 января 2021 года по 2025 год, планируется приобрести 88 006 единиц медицинского оборудования и 19 080 единиц автотранспорта.
Журнал "Медицинские изделия". Российский рынок медицинских изделий. Итоги 2020 года, декабрь 2020 г.