- Главная
- Регуляторный консалтинг
- Сопровождение государственной регистрации
Сопровождение государственной регистрации медицинских изделий в России
Государственная регистрация является обязательной процедурой, необходимой для легального обращения на территории РФ как российских, так и зарубежных медизделий. После успешного прохождения процедуры государственной регистрации, ранее на медицинское изделие выдавалось регистрационное удостоверение Росздравнадзора. Однако, с 1 марта 2025 года, согласно ПП РФ № 1684, бумажный бланк регистрационного удостоверения заменен реестровой записью.
Комплексное сопровождение государственной регистрации российских медизделий включает:
- Первичную оценку документов и внесение исправлений, при необходимости;
- Подготовку и организацию токсикологических испытаний;
- Подготовку и организацию технических испытаний;
- Подготовку и подачу регистрационного досье в Росздравнадзор;
- Проработку замечаний от экспертной организации;
- Подготовку к проведению клинических испытаний;
- Возобновление процесса регистрации (подача результатов клинических испытаний);
- Получение регистрационного удостоверения Росздравнадзора.
Для медицинских изделий зарубежного производства дополнительно выполняется:
- Получение разрешения на ввоз образцов;
-
Организация и проверка перевода документации на медизделие.
Сроки прохождения процедуры государственной регистрации:
- для изделия класса 1 риска - от 8 месяцев;
-
для изделия класса риска 2а, 2б, 3 - от 12 месяцев.
Стоимость услуг и сроки прохождения процедуры регистрации могут отличаться в зависимости от вида медизделия, класса риска, типа документации, которую необходимо разработать и других факторов.
До 31 декабря 2027 года продлена возможность регистрации медизделий в соответствии с законодательством государства-члена ИЛИ по правилам Евразийского экономического союза.
СПРАВОЧНАЯ ИНФОРМАЦИЯ:
Государственная регистрация медицинских изделий в РФ осуществляется регистрирующим органом — Федеральной службой по надзору в сфере здравоохранения (Росздравнадзор).
После успешного прохождения процедуры государственной регистрации, сведения о зарегистрированном изделии вносятся в "Государственный реестр медицинских изделий и организаций (индивидуальных предпринимателей), осуществляющих производство и изготовление медицинских изделий".
Регистрация медицинского изделия в Росздравнадзоре невозможна без полного пакета технической и эксплуатационной документации, в том числе файла менеджмента риска.
Этапы государственной регистрации медицинских изделий
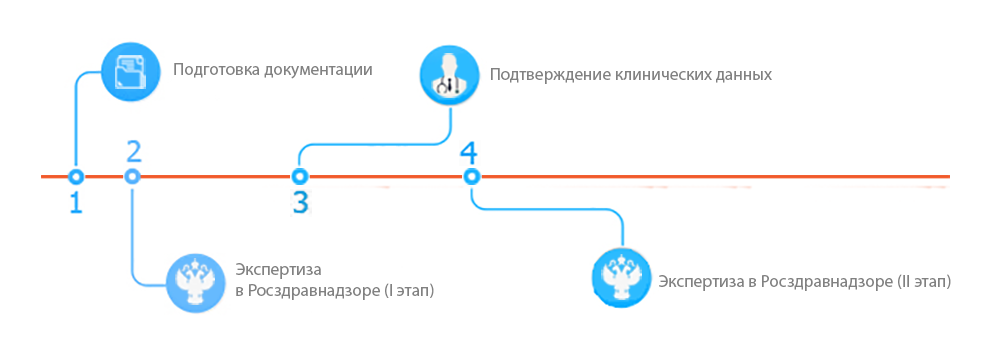
1. Подготовка документации
1.1. Первичная оценка документации на соответствие требованиям Росздравнадзора.
1.2. Корректировка документации в соответствии требованиям Росздравнадзора.
1.3. Получение разрешения на ввоз образцов (только для изделий зарубежного производства)
1.4. Испытания
1.4.1. Проведение токсикологических испытаний
1.4.2. Проведение технических испытаний.
1.5. Формирование и подача досье в Росздравнадзор.
2. Экспертиза в Росздравнадзоре (I этап)
2.1. Комплект регистрационной документации в Росздравнадзоре проходит проверку полноты и достоверности предоставленных сведений.
2.2. Экспертиза качества, эффективности и безопасности проводится экспертной организацией в срок не превышающий 20 рабочих дней.
2.3. По окончании экспертизы составляется заключение о возможности (невозможности) проведения клинических исследований (для медицинских изделий класса риска 2а, 2б и 3).
3. Подтверждение клинических данных
3.1. Проведение клинических испытаний
3.2. Подача клинических данных
4. Экспертиза в Росздравнадзоре (II этап)
4.1. Экспертиза клинических данных в срок не превышающий 10 рабочих дней
4.2. По окончании экспертизы принимается решение о выдачи регистрационного удостоверения
Примечание: I и II этап экспертизы для медицинских изделий 1 класса риска и in vitro объединены
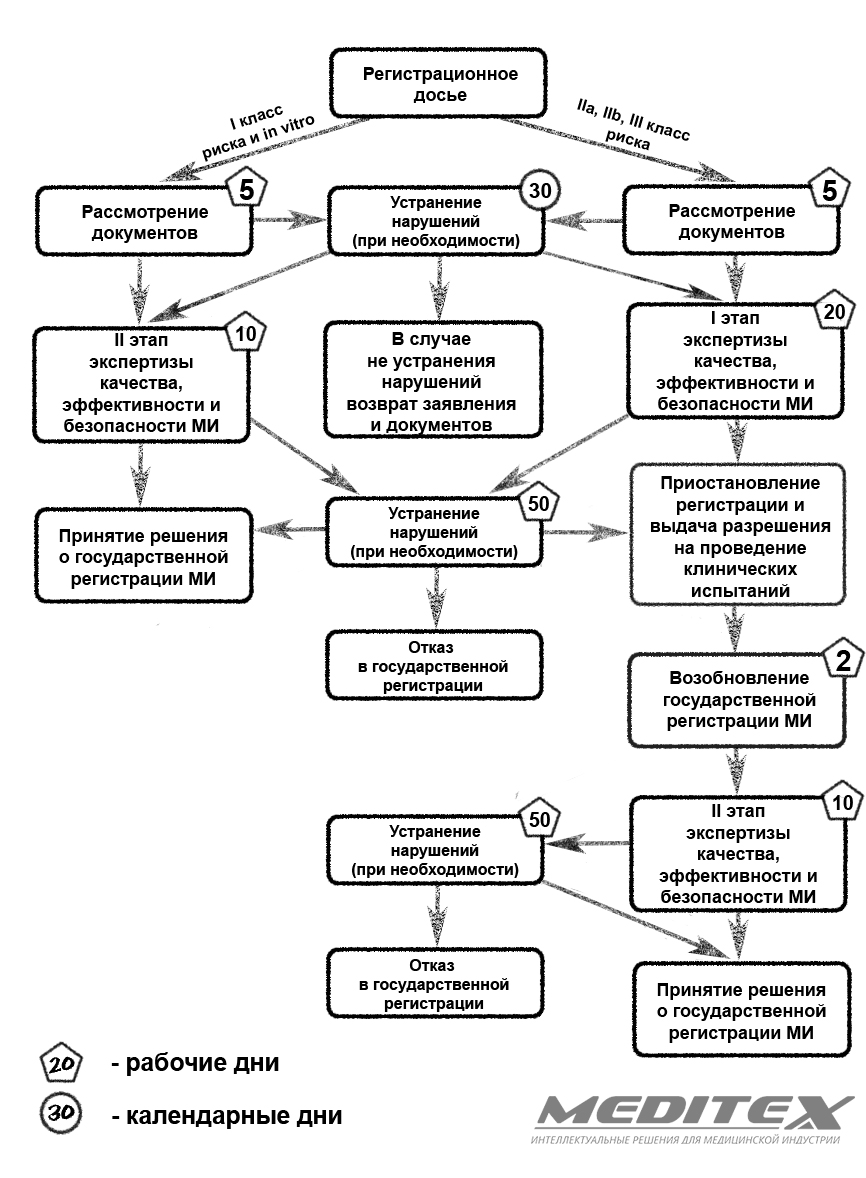
Классы риска изделий
В соответствии с приказом Министерства здравоохранения от 6 июня 2012 г. N 4н медицинские изделия в зависимости от потенциального риска применения подразделяются на четыре класса. Классы имеют обозначения:
класс 1 - медицинские изделия с низкой степенью риска;
класс 2а - медицинские изделия со средней степенью риска;
класс 2б - медицинские изделия с повышенной степенью риска;
класс 3 - медицинские изделия с высокой степенью риска.
Классификация медицинских изделий для диагностики in vitro:
класс 1 - медицинские изделия с низким индивидуальным риском и низким риском для общественного здоровья;
класс 2а - медицинские изделия с умеренным индивидуальным риском и/или низким риском для общественного здоровья;
класс 2б - медицинские изделия с высоким индивидуальным риском и/или умеренным риском для общественного здоровья;
класс 3 - медицинские изделия с высоким индивидуальным риском и/или высоким риском для общественного здоровья.
Размер государственной пошлины
В соответствии с классом определяется размер государственной пошлины за проведение экспертизы качества, эффективности и безопасности медицинских изделий.
класс 1 - 45 000 рублей;
класс 2а - 65 000 рублей;
класс 2б - 85 000 рублей;
класс 3 - 115 000 рублей.
>> Списки документов для регистрации медицинских изделий >>
>> Нормативные документы по регистрации медицинских изделий >>
>> Бланки государственных пошлин >>

