Обзор подготовлен по данным Реестра российской промышленной продукции - https://gisp.gov.ru/pp719v2/pub/prod/. Ведение реестра осуществляется в Государственной информационной системе промышленности (ГИСП).
Дата выгрузки: 5 декабря 2025 года. На указанную дату в реестре было 36 522 действующие записи о медицинских изделиях, признанных российской продукцией. Данные в реестре относятся к 2022-2025 годам.
Для отбора данных о медицинских изделиях, внесенных в реестр, были проанализированы данные из справочника кодов ОКПД 2. Анализ показал, что записи о медицинских изделиях вносились в реестр следующими департаментами Минпромторга РФ:
|
Наименование департамента Минпромторга РФ |
Количество внесенных записей |
| Департамент развития фармацевтической и медицинской промышленности |
29 995 |
|
Департамент развития промышленности социально-значимых товаров |
2 463 |
| Департамент легкой промышленности и лесопромышленного комплекса |
1 931 |
|
Департамент радиоэлектронной промышленности |
1 290 |
|
Департамент химической промышленности |
694 |
| Департамент химико-технологического комплекса и биоинженерных технологий |
138 |
|
Департамент государственной политики в области технического регулирования, стандартизации |
2 |
|
Управление государственной политики в области технического регулирования, стандартизации и обеспечения единства измерений |
2 |
Для 7 записей наименование департамента в реестре не указано.
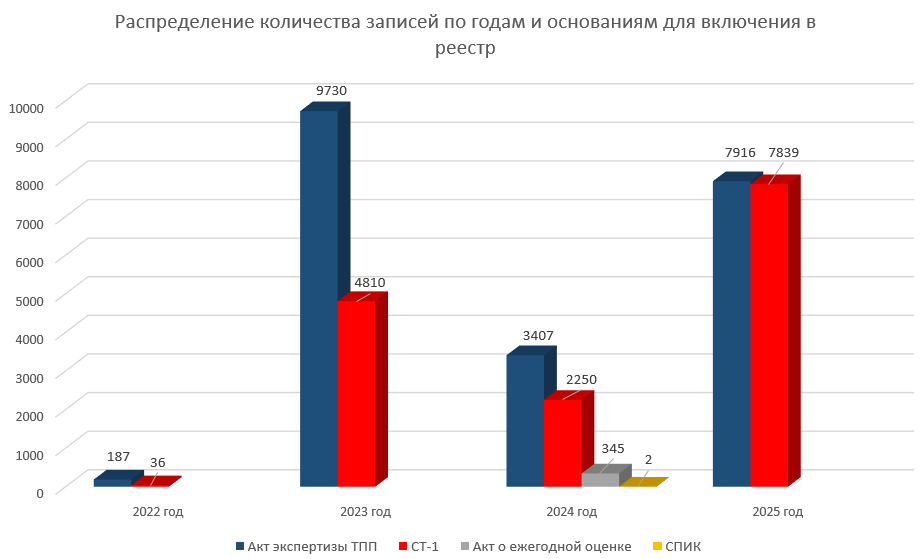
Первые записи о получении статуса «российской продукции» датированы в Реестре 2022 годом. В указанный период было внесено 223 записи.
В 2023 году в реестр было внесено уже 14 540 записей. Основная часть записей (67%) вносилась на основании «акта экспертизы торгово-промышленной палаты (ТПП)».
Акт экспертизы ТПП - это документ, подтверждающий выполнение требований Постановления № 719 (17.07.2015).
Сертификат СТ-1 также подтверждает страну происхождения товара, но по более мягким, чем балльная оценка, критериям стран СНГ. И не отражает глубину локализации.
В 2024 году количество вносимых в Реестр записей сократилось до 6 004. При этом в данный год появились новые основания для внесения информации о медизделиях в реестр: «акт о ежегодной проверке» и «СПИК».
Акт о ежегодной проверке — это документ, который подтверждает, что производитель, уже включенный в Реестр, сохранил свои производственные мощности и продолжает соблюдать требования локализации. Появление данного документа было связано с изменениями правил выдачи заключения ТПП (оно стало выдаваться на 3 года, но производитель обязан ежегодно подтверждать свой статус).
На основании «акта о ежегодной проверке» был продлен срок действия документов о локализации по 345 записям. Однако затем было принято решение, при котором в случае продления срока действия «акта экспертизы ТПП», данный акт остается указанным в качестве основания внесения данных в Реестр, и меняется только дата внесения данных и срок действия акта.
Таким образом, часть записей (не более 4,5%), внесенных в реестр в 2024 и 2025 годах, является результатом продления сроков действия «актов экспертизы ТПП», полученных предприятиями ранее.
В 2024 году «Акт экспертизы ТПП» по-прежнему являлся наиболее частым основанием для внесения записей в реестр - 57% записей.
Участие производителя в реализации специального инвестиционного контракта (СПИК) стало основанием для внесения данных о производимой продукции только для 2 видов медицинских перчаток, выпускаемых НАО «Нитриленд».
В 2025 году отмечался существенный рост количества внесенных в Реестр записей – 15 755. Также важным изменением является увеличение количества выданных сертификатов СТ-1. В указанном периоде сертификат СТ-1 стал основанием для внесения 49% записей в реестр.
Данное явление получило название «бумажной локализации». Поскольку рост количества таких записей в Реестре не свидетельствует о росте количества действительно локализованных в стране производств.
Отметим основные нормативные правовые акты, которые могли повлиять на волнообразное наполнение реестра ГИСП.
| Постановление | Содержание | Влияние на реестр |
| Постановление Правительства № 719 (17.07.2015) | Определяет критерии локализации и закладывает основы балльной системы | Фундамент для создания реестра |
| Постановление Правительства № 102 (05.02.2015) | Правило «третий лишний» | Драйвер получения подтверждения страны происхождения для массовых медизделий |
| Приказ Минпромторга № 1755 (29.05.2020) | Закрепил процедуру ведения реестра | С января 2021 г. оформление подтверждения локализации осуществляется через личный кабинет на портале ГИСП |
| Постановление Правительства № 1432 (28.08.2021) | Расширение «второго лишнего» на 30+ видов медизделий | Появление записей в реестре (2022 год) |
| Постановление Правительства РФ №552 (01.04.2022) | Приостановлено действие положений ПП № 719 о переходе на балльную систему с 2022 года. | Часть производителей занимают выжидательную позицию |
|
Постановление Правительства № 2519 (29.12.2022) Постановление Правительства № 1293 (08.08.2023) |
Введена балльная система для 24 видов медизделий. Введена балльная система еще для 18 видов медизделий. |
Рост количества записей в Реестре за 2023 год |
| 2024 года. Адаптация к сформированной системе. | Снижение общего количества новых записей | |
|
Постановление Правительства № 901 (16.06.2025) Постановление Правительства № 2225 (30.12.2025) |
Ужесточение правил локализации. Ввод обязательной балльной системы для большинства медизделий и средств реабилитации с 1 января 2026 года. До 30 ноября 2026 года продлен переходный период, когда допускается использование реестровых записей без указания баллов. |
Рост количества записей в 2025 году (особенно во второй половине года) |
Необходимо отметить, что в случае, когда документы, подтверждающие страну происхождения медизделия, были получены в конце календарного года, информация о них может быть внесена в реестр в начале следующего года. Например, в 2022 году таких записей было около 100 (около 30%).
Также необходимо учитывать временной лаг, между публикацией того или иного Постановления Правительства, принятием решения производителем о дальнейших действиях и сроком получения подтверждения статуса российской продукции на свою продукцию.
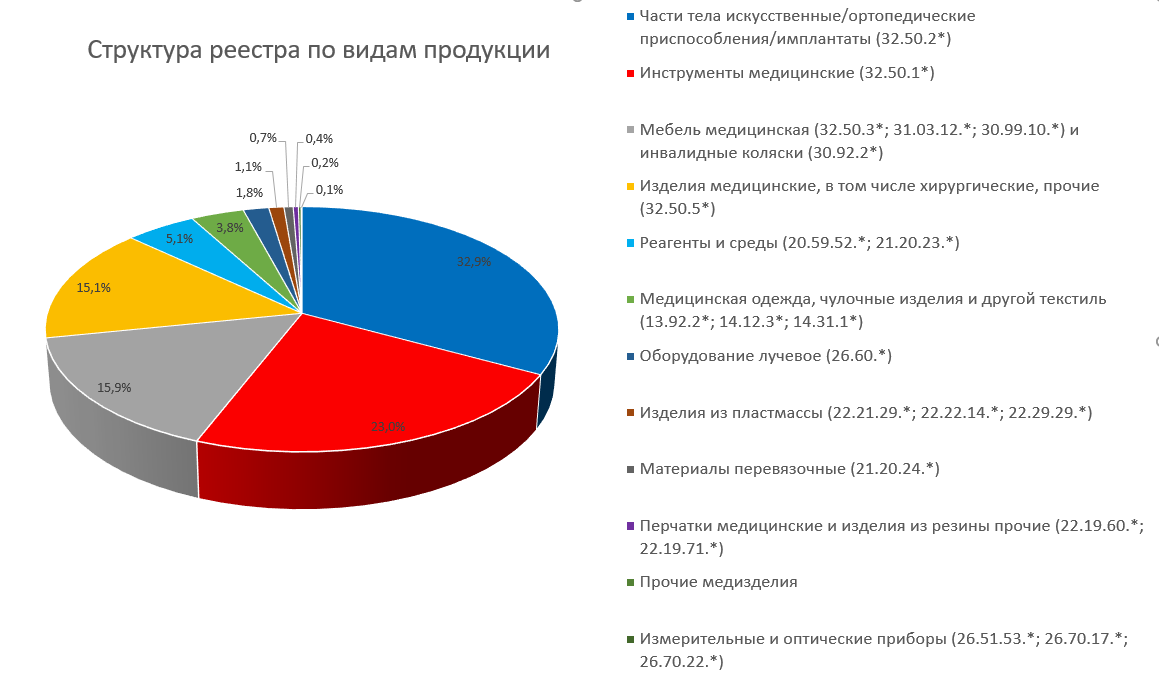
Представленные в реестре записи можно условно разделить на 12 товарных групп:
В количественном выражении более 50% записей приходится на изделия первых двух групп. Существенную долю также составляют группы «медицинская мебель, инвалидные кресла» и «изделия медицинские, в том числе хирургические, прочие».
А вот доля группы «измерительные и оптические приборы» составляет менее 0,1%. Также невелика доля «лучевого оборудования», которое в стоимостном выражении является одним из ключевых сегментов рынка медицинских изделий.
Для большей наглядности дополнительно приведем данные о распределении количества записей в Реестре по наиболее востребованным кодам ОКПД 2 за каждый год.
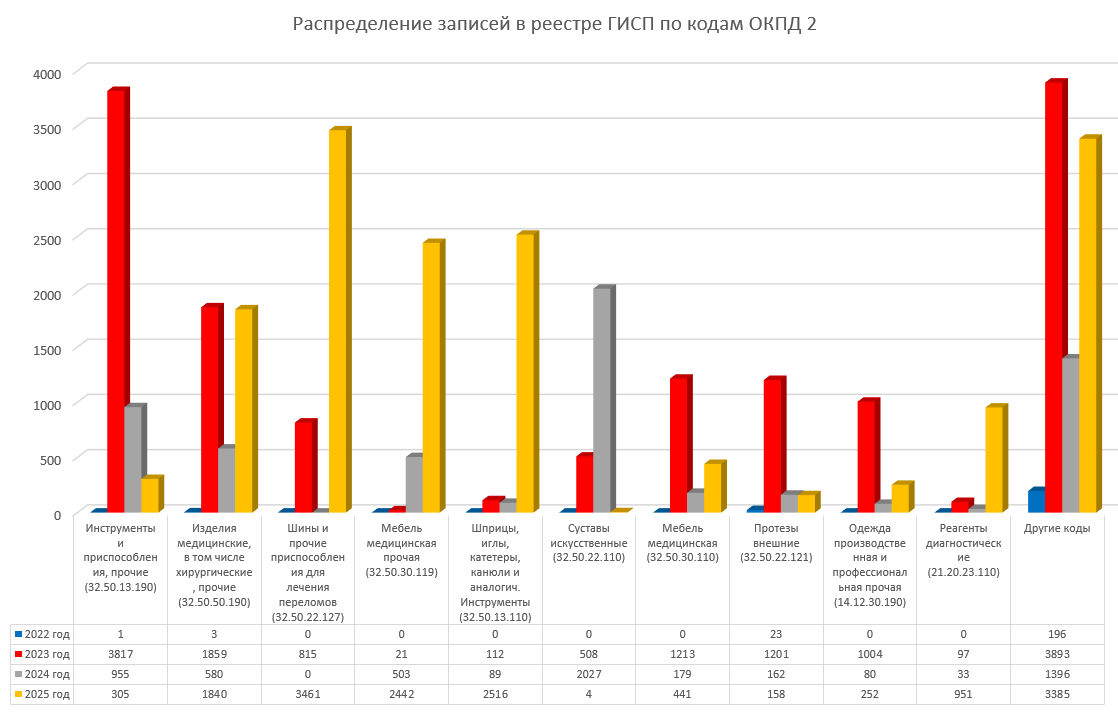
Как видно из данных диаграммы, в 2023 году подтверждение страны происхождения чаще всего получали для изделий по следующим кодам ОКПД 2:
Все эти изделия подпадают под правило «третий лишний», таким образом, без включения в Реестр промышленной продукции производители данной продукции потеряли бы возможность участвовать в госзакупках.
В 2024 году подтверждение страны происхождения было наиболее востребовано для искусственных суставов. А в 2025 году для изделий по следующим кодам ОКПД 2:
Необходимо отметить, что все 36,5 тысячи записей в реестр внесены 470 производителями. Ниже представлена информация о 15 производителях, которые наибольшее количество раз получили подтверждение российского статуса для своей продукции.
| Наименование производителя |
Количество записей, внесенных в реестр |
|
ООО "АНАТОМИКА" - имплантаты, инструменты для остеосинтеза и спинальной хирургии, а также эндопротезы крупных суставов |
5 198 |
|
ООО "МЕДИКО-ИНСТРУМЕНТАЛЬНЫЙ ЗАВОД ТУМБОТИНО" - многоразовый медицинский инструмент и мебель |
2 743 |
|
АО "МОСКОВСКОЕ ПРОТЕЗНО-ОРТОПЕДИЧЕСКОЕ ПРЕДПРИЯТИЕ" - протезно-ортопедические изделия |
2 609 |
|
ООО "ПРОИЗВОДСТВЕННО-ТЕХНИЧЕСКОЕ ОБЪЕДИНЕНИЕ "МЕДТЕХНИКА" - медицинские изделия для хирургии и остеосинтеза на основе титановых сплавов и нержавеющей стали |
2 549 |
|
ООО "ОСТЕОМЕД-М" - имплантаты и инструменты для травматологии, ортопедии, эндопротезирования и спинальной хирургии |
1 630 |
| ООО "МЕДСТАЛЬКОНСТРУКЦИЯ" - медицинская и металлическая мебель |
801 |
| ООО "ГРАНАТ БИО ТЕХ" - вакуумные системы взятия венозной крови |
684 |
| ООО МЕДИЦИНСКАЯ КОМПАНИЯ "АСК" - медицинская мебель и оборудование |
631 |
| ООО "ДОКТОР МЕБЕЛЬ" - специализированная медицинская и лабораторная мебель |
614 |
|
ООО "ХОЛДИНГОВАЯ КОМПАНИЯ "ИНТЕГРАЛ" – медицинские инструменты и оборудование |
605 |
| НАО "ПЕРИНТ" - медицинские расходные материалы и пластиковая упаковка |
530 |
|
АО "ЗАВОД МЕДИЦИНСКИХ ТЕХНОЛОГИЙ" - бельё хирургическое одноразовое стерильное, одежда и расходные материалы для лабораторий |
519 |
| ООО "МЕДИЦИНОФФ" - медицинские инструменты и оборудование |
482 |
| ООО "КОМПАНИЯ ВИЦЫАН" – медицинские матрасы, ортопедические подушки, средства реабилитации |
476 |
| ООО "ВАЛИДУС" - медицинская и лабораторная мебель |
466 |
Отметим, что у ООО "АНАТОМИКА" более 5 тысяч действующих записей в реестре, подтверждающих локализацию своей продукцию. Это составляет чуть больше 14% от всех записей реестра. Столь высокая доля одного игрока создаёт системный риск: любые форс-мажорные обстоятельства у данного производителя (смена собственника, производственный сбой) существенно затронут государственный сектор российского рынка имплантатов.
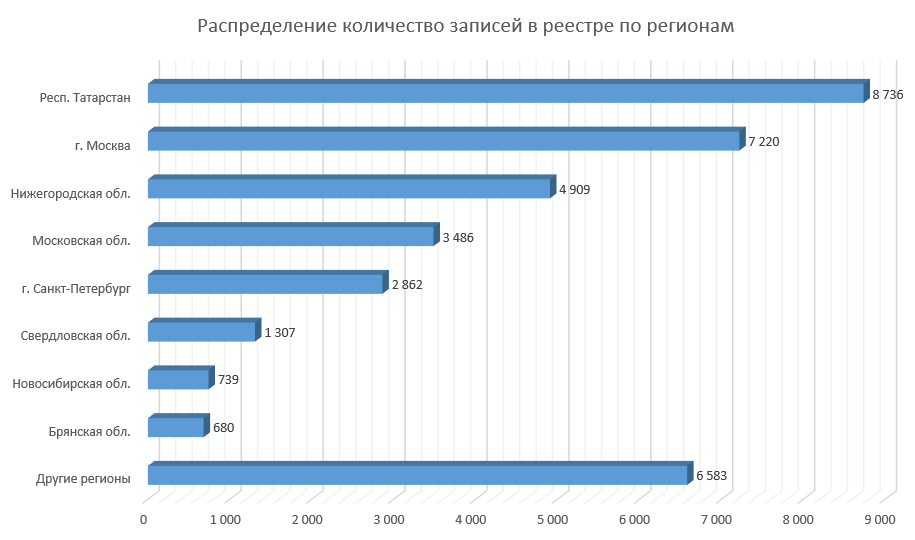
Анализ регионального распределения количества записей в реестре ГИСП показывает лидирующие позиции трех регионов: республика Татарстан, город Москва и Нижегородская область. Производители из данных регионов сформировали более 57% записей реестра. Это свидетельствует о высокой географической концентрации, в рамках Реестра, и не позволяет объективно оценить производственный потенциал остальных субъектов РФ.
Проведенный анализ показал, что динамика реестра определяется не рыночными факторами, а административными циклами: каждое крупное изменение нормативной базы вызывает волну новых записей, подтверждающих страну происхождения продукции, с временным лагом.
Важной особенностью рынка является высокая степень его концентрации, согласно анализу товарных категорий, ведущих производителей и регионов.
Прогнозируя развитие реестра в 2026 году, отметим, что сертификаты СТ-1, количество которых особенно возросло в 2025 году, будут признаны недействительными после окончания переходного периода и введения обязательной балльной системы оценки локализации для новых групп медицинских изделий.
Реестр ГИСП содержит специальные маркеры: «Искусственный интеллект» и «Высокотехнологичное оборудование». Анализ данных показал, что в настоящее время ни один вид продукции из 36 522 записей, не получил подтверждение по данным критериям.
Оценивать данный факт можно и как свидетельство низкого уровня технологической сложности локализованного производства, и как подчеркнутую важность появления таких изделий для регулятора. Его готовность предоставлять дополнительные преференции данным производителям.
В заключение отметим, что выполненный анализ является упрощенной версией, поскольку оценка количества записей в той или иной категории не отражает стоимость разных изделий.
Для одних категорий необходимо подтверждать российский статус для каждого типоразмера продукции, а в другой категории одной записью подтверждается локализованное производство компьютерного томографа.
Однако, выполненная нами глубокая переработка Реестра ГИСП, в том числе с использованием технологий ИИ, позволяет предлагать своим партнерам профессиональную (более объективную) версию отчета, по выбранному сегменту рынка.
Предоставляемая по запросу версия отчета дополнительно включает оценку применения балльной системы в сегменте, соотношение государственного и частного капитала, поквартальную динамику наполнения реестра, расчет коэффициентов концентрации и объема годового роста.
Использование материалов отчета допускается только с указанием ссылки на источник.